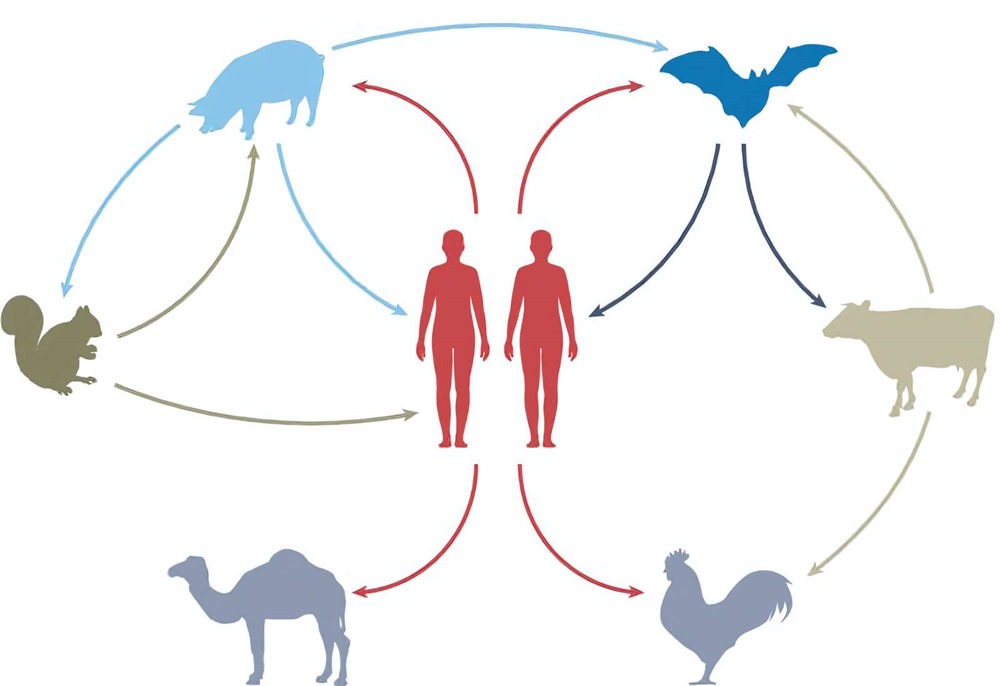
Les humains propagent davantage de virus aux autres animaux qu’ils ne nous en transmettent
L‘effroyable pandémie de COVID a mis en lumière des conséquences zoonotiques. La théorie la plus répandue veut que le SRAS-CoV-2, le virus responsable de la COVID-19, ait muté chez les chauves-souris et se soit ensuite propagé à d’autres animaux sauvages vendus vivants pour la nourriture sur les marchés de Wuhan, où ils ont fini par infecter des êtres humains.
Image d’entête : la toile du transfert viral. (Tan et al./Nature Ecology & Evolution)
Cela n’aurait pas dû être une surprise, car nous avons déjà dû faire face à de nombreuses zoonoses, d’Ebola aux grippes aviaire et porcine. Mais il est facile d’oublier que les microbes ne font pas le saut entre les espèces dans une seule direction. Il s’agit toujours d’une voie à double sens, et cette dynamique peut être étonnante. Des chercheurs de l’University College de Londres (UCL) ont récemment étudié la dynamique virale dans des détails sans précédent, révélant un fait révélateur : les humains transmettent aux animaux domestiques et sauvages deux fois plus de virus qu’ils n’en attrapent d’eux.
La zooanthroponose, c’est-à-dire le passage de virus des humains à d’autres animaux, est de plus en plus souvent détectée. Les épidémies de grippe A (H1N1) de 2009 chez les porcs et les épidémies de SRAS-CoV-2 chez des populations d’animaux sauvages sont des exemples de ces événements « zoonotiques inversés ». Les propriétaires d’animaux de compagnie sont peut-être plus conscients de cette dynamique, car il est courant que les chiens, les chats et même les furets présentent des symptômes semblables à ceux de la grippe après avoir été en contact avec des humains infectés.
L’importance de la source virale humaine n’a jamais été clairement établie. Et, bien entendu, ce type de recherche a tendance à se concentrer sur la transmission de l’animal à l’homme. Pour leur étude, les chercheurs se sont attelés à la tâche herculéenne d’analyser près de 12 millions de génomes viraux. Ceux-ci ont été utilisés pour construire des arbres phylogénétiques qui les ont aidés à trouver des modèles de “sauts/ tranmissions d’hôte” antérieurs. Imaginons un scénario dans lequel un virus est présent à la fois chez la chauve-souris et chez l’humain, et où les souches virales de ces deux hôtes ne diffèrent que par quelques mutations. Cette similitude suggère un événement de transmission récent. Mais la question cruciale est la suivante : qui a infecté qui ? C’est à cela que servent les arbres phylogénétiques. Ce sont essentiellement des arbres généalogiques pour les virus. En cartographiant les relations évolutives entre les différentes souches virales, il est possible de trouver leurs ancêtres communs. Ces arbres permettent également aux scientifiques de déduire la direction du saut d’un hôte viral.
Selon Balloux :
Si nous trouvons des clades bien étayés de souches provenant toutes de l’espèce hôte A au sein d’un clade de l’espèce hôte B, nous pouvons être presque sûrs que le virus a sauté de l’hôte B à l’hôte A.
Ce n’était pas une tâche triviale. Le volume de données lui-même est immense. Pour compliquer encore les choses, la diversité écologique des virus était beaucoup plus riche que ce qui avait été classifié auparavant à l’aide de méthodes conventionnelles. Pour surmonter ce problème, les chercheurs ont construit leur propre arbre phylogénétique comprenant 32 familles de virus sur la base de la seule parenté génétique. L’autre problème assez frustrant fut le manque de métadonnées à la disposition des chercheurs. De nombreux génomes viraux soumis aux bibliothèques ne contenaient pas d’informations essentielles telles que la date, le lieu et l’hôte sur lequel le virus avait été prélevé.
Grâce à cette minutieuse reconstruction de l’histoire évolutive des virus et à l’examen des mutations génétiques acquises lors des sauts d’hôte, les chercheurs ont remis en question la notion selon laquelle l’humain n’est qu’un point d’aboutissement pour les maladies virales. Leur plus étonnante découverte est que les événements de transmission de l’humain à l’animal sont environ deux fois plus fréquents que l’inverse. Les sauts d’hôte d’animal à animal qui n’impliquent pas l’humain sont encore plus fréquents. Cela souligne une fois de plus le fait que l’humain n’est jamais en dehors de la nature, même si notre orgueil peut nous amener à penser le contraire. Au contraire, nous faisons partie intégrante d’un écosystème complexe, échangeant sans cesse des agents pathogènes avec d’autres espèces.
Les auteurs de l’étude se sont également penchés sur les fondements génétiques de ces “sauts de l’hôte”. Ils ont constaté que les virus subissent souvent des mutations importantes lorsqu’ils s’adaptent à de nouveaux hôtes. Il est intéressant de noter que les virus ayant un large éventail d’hôtes animales présentaient moins de signes de telles mutations adaptatives. Il semblerait qu’il y ait une polyvalence inhérente à l’infection de diverses espèces.
Toujours selon Balloux :
Un autre résultat intéressant est que les virus ayant une large gamme d’hôtes nécessitent moins de changements évolutifs pour s’adapter à un nouvel hôte. Cela explique probablement le schéma bien connu selon lequel les virus les plus préoccupants en tant qu’agents possibles d’épidémies et de pandémies ont tendance à être des généralistes capables d’infecter plusieurs hôtes.
L’une des premières étapes pour mieux comprendre l’impact de ces sauts d’hôte consiste à renforcer les efforts de surveillance génomique chez les espèces animales domestiques et sauvages, ce qui nous aiderait à évaluer la diversité des virus infectant les animaux, la fréquence des sauts d’hôte et le risque d’émergence ou de réémergence de maladies infectieuses chez ces animaux.
La zoonose inversée, la zooanthroponose, pourrait également rendre plus probables les épidémies chez l’humain. Des virus entièrement nouveaux peuvent apparaître à la suite d’une mutation ou d’un échange de matériel génétique entre différents virus infectant un hôte au même moment. Ce dernier processus, connu sous le nom de recombinaison virale, est particulièrement risqué. La circulation de virus humains à partir de porcs, qui agissent comme des récipients de mélange qui peuvent ensuite transmettre de nouvelles souches mutées à l’humain, en est l’un des exemples les plus frappant. En 2009, le virus de la grippe H1N1 a tué entre 151 700 et 575 400 personnes dans le monde au cours de sa première année d’existence. Mais ce virus, qui est passé de l’animal à l’humain, comprenait des segments de gènes provenant de quatre origines différentes : l’humain, l’oiseau, le porc d’Amérique du Nord et le porc d’Eurasie.
On ne sait toujours pas dans quelle mesure les zoonoses inversées augmentent le risque de pandémies ou d’épidémies majeures à plus grande échelle. La majorité des maladies zoonotiques émergentes sont apparues chez des animaux sauvages, et non chez des animaux d’élevage ou de compagnie. Toutefois, les interactions entre l’humain et les autres espèces sont incroyablement complexes, ce qui justifie une surveillance génomique beaucoup plus poussée que celle qui existe actuellement.
L’étude publiée dans Nature Ecology & Evolution : The evolutionary drivers and correlates of viral host jumps et présentée sur le site de l’University College de Londres : Humans pass more viruses to other animals than we catch from them.