Des bactéries intestinales pourraient être à l’origine de la cécité due à certaines maladies oculaires
Des recherches suggèrent que des maladies oculaires longtemps considérées comme purement génétiques pourraient être causées en partie par des bactéries qui s’échappent de l’intestin et se déplacent jusqu’à la rétine.
Des chercheurs chinois et britanniques ont découvert des bactéries de l’intestin dans des zones endommagées des yeux de souris présentant des mutations du gène Crumbs homolog 1 (CRB1), une cause majeure de maladies oculaires héréditaires.
Selon l’ophtalmologiste Richard Lee, de l’University College de Londres, l’un des principaux auteurs de l’étude :
Nous avons découvert un lien inattendu entre l’intestin et l’œil, qui pourrait être la cause de la cécité chez certains patients. Nos résultats pourraient avoir d’énormes répercussions sur la transformation du traitement des maladies oculaires associées à CRB1.
Il s’agit de recherches préliminaires et nous ne savons pas si le même mécanisme se produit chez les humains porteurs de la mutation CRB1, qui est à l’origine de 4 % des rétinites pigmentaires, entraînant une perte de la vision périphérique et nocturne, et de 10 % des amauroses congénitales de Leber, qui entraînent une cécité complète dans environ un tiers des cas.
Dans les maladies oculaires associées à CRB1, la déficience visuelle commence dès le plus jeune âge. La rétine, le tissu situé à l’arrière de nos yeux qui convertit les longueurs d’onde de la lumière en signaux que notre cerveau interprète comme la vision, ne parvient pas à développer sa fine structure de cellules photoréceptrices sensibles à la lumière et devient anormalement épaisse.
L’équipe s’est demandé si les bactéries étaient à l’origine des lésions rétiniennes après avoir constaté, lors de précédentes recherches, que les bactéries étaient étonnamment répandues dans les yeux. La plupart de nos milliards de bactéries intestinales sont utiles plutôt que nocives et jouent un rôle crucial dans la santé générale. Mais Lee et ses collègues pensent que la mutation CRB1 permet aux bactéries intestinales d’atteindre les yeux, où elles peuvent contribuer à une perte de vision.
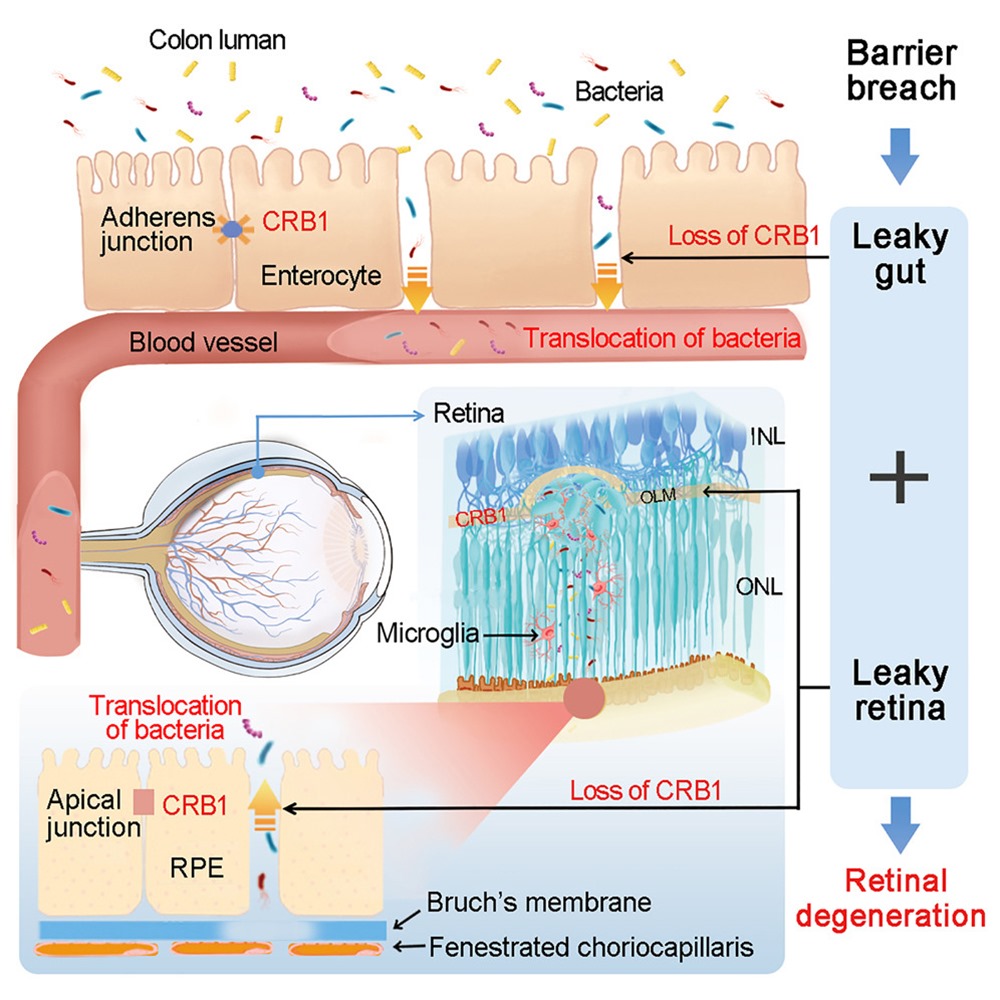
La protéine Crb1 codée par le gène était censée se trouver uniquement dans le cerveau et l’épithélium pigmentaire rétinien (EPR), la barrière externe sang-rétine qui protège l’œil. Pour la première fois, les chercheurs ont découvert que la paroi intestinale exprime également cette protéine. Elle est essentielle au maintien d’une barrière entre l’intestin et le reste du corps, et l’EPR. Un gène CBR1 muté n’exprime pas suffisamment la protéine Crb1, ce qui entraîne des brèches dans ces deux barrières protectrices.
Les modèles de souris porteurs de la mutation présentaient des déficiences au niveau de ces deux barrières, ce qui permettait aux bactéries intestinales de passer dans la rétine à travers la circulation sanguine et de provoquer des lésions. Un traitement antibiotique a permis de réduire les lésions rétiniennes et de prévenir la perte de vision. Lorsque les chercheurs ont réintroduit l’expression normale de Crb1 dans l’intestin des souris porteuses de la mutation CRB1, ils n’ont pas réussi à inverser la rupture de la barrière, mais les lésions de la rétine ont été réduites. Les souris mutées CRB1 dont les populations bactériennes étaient réduites ne présentaient pas non plus autant de lésions rétiniennes.
A partir de l’étude : résumé de la façon dont la mutation de CRB1 permet aux bactéries intestinales d’accéder à la rétine. (Peng et col./ Cell)
Nous espérons poursuivre ces recherches dans le cadre d’études cliniques afin de confirmer si ce mécanisme est effectivement à l’origine de la cécité chez les humains, et si des traitements ciblant les bactéries pourraient prévenir la cécité.
Cela ne fait que suggérer un lien possible entre les maladies oculaires causées par la mutation du gène CRB1. Près de 100 gènes affectant les cellules photoréceptrices sensibles à la lumière de la rétine peuvent causer la rétinite pigmentaire, et des variantes dans au moins 28 gènes peuvent entraîner l’amaurose congénitale de Leber.
La thérapie génique s’est révélée prometteuse dans le traitement des maladies oculaires génétiques et elle a été jusqu’à présent l’un des principaux axes de développement des traitements. Cependant, en 2023, des scientifiques ont établi un lien entre des cellules immunitaires spécifiques migrant de l’intestin vers la rétine et la gravité du glaucome.
Les auteurs affirment que leurs résultats montrent que l’intestin et l’œil sont liés d’une autre manière : des bactéries vivantes peuvent migrer d’un intestin qui fuit vers la rétine. Nous ne comprenons pas encore parfaitement le lien entre l’intestin et la santé oculaire, mais il pourrait s’agir d’une autre voie de traitement à envisager.
Lee de conclure :
Comme nous avons révélé un mécanisme entièrement nouveau reliant la dégénérescence rétinienne à l’intestin, nos résultats peuvent avoir des implications pour un spectre plus large de pathologies oculaires, que nous espérons continuer à explorer par d’autres études.
L’étude publiée dans la revue Cell : CRB1-associated retinal degeneration is dependent on bacterial translocation from the gut et présentée par University College de Londres via Eurekalert : Blindness from some inherited eye diseases may be caused by gut bacteria.