Des chercheurs ne s’attendaient pas à améliorer les performances d’une enzyme ayant le pouvoir de transformer nos déchets plastiques
Notre problème de pollution plastique ne fait qu’empirer, mais les scientifiques pourraient bientôt disposer d’un nouvel outil pour s’attaquer au problème. Avec un peu de chance, des chercheurs ont découvert une enzyme modifiée qui a un appétit pour certains types de nos plastiques qui ce retrouve dans la nature, ce qui signifie que ces déchets pourraient être décomposés relativement rapidement sans contaminer l’environnement pendant des centaines d’années.
Nous produisons des centaines de millions de tonnes de polyéthylène téréphtalate (PET) chaque année pour les bouteilles de soda et de shampoing. Une petite partie de ces déchets est recyclée, ce qui signifie que nous polluons notre environnement avec des matériaux qui mettent des siècles à se dégrader, dont une grande partie est rejetée dans l’océan où ils se fragmentent en petits morceaux qui sont presque impossibles à suivre, et encore moins à nettoyer.
Les scientifiques ont fait de prometteuses découvertes lorsqu’il s’agit de mettre des organismes vivants au travail sur ce dilemme, avec les vers de cire et les bactéries, pour ne citer que quelques exemples récents. Les scientifiques de l’université de Portsmouth et du National Renewable Energy Laboratory (NREL) du département de l’Énergie des États-Unis ont utilisé cette enzyme récemment découverte, qui consomme des plastiques PET appelés PETase, comme point de départ de leurs recherches révolutionnaires.
Les chercheurs ont entrepris de mieux comprendre la structure cristalline de la PETase, dont on pense qu’elles se seraient développées dans un centre de recyclage japonais, d’où ses capacités à transformer le plastique. Cette étrange enzyme, provient de la bactérie Ideonella sakaiensis, et elle décompose les PET en acide téréphtalique et en éthylène glycol dans un processus qui prend des jours plutôt que des siècles.
Ce qui intéressait les scientifiques, c’était l’évolution de l’enzyme, étant donné que les plastiques PET existaient dans l’environnement que depuis les années 1940 et que s’ils pouvaient comprendre comment cela s’est produit dans un laps de temps relativement court, ils pourraient peut-être savoir comment la rendre plus efficace pour manger du plastique.
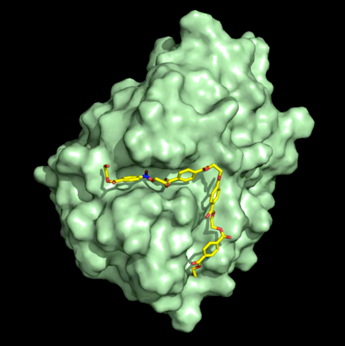 Ils ont commencé par utiliser un synchrotron à l’installation Diamond Light Source au Royaume-Uni, ce qui leur a permis de voir les atomes individuels à l’intérieur de la structure de l’enzyme en les bombardant avec des faisceaux de rayons X 10 milliards de fois plus brillants que le soleil. Grâce à cette méthode, ils se sont retrouvés avec un modèle 3D à ultra-haute résolution de la PETase que vous pouvez admirer ci-contre.
Ils ont commencé par utiliser un synchrotron à l’installation Diamond Light Source au Royaume-Uni, ce qui leur a permis de voir les atomes individuels à l’intérieur de la structure de l’enzyme en les bombardant avec des faisceaux de rayons X 10 milliards de fois plus brillants que le soleil. Grâce à cette méthode, ils se sont retrouvés avec un modèle 3D à ultra-haute résolution de la PETase que vous pouvez admirer ci-contre.
Selon le professeur John McGeehan de l’université de Portsmouth :
La Diamond Light Source a récemment créé l’un des faisceaux de rayons X les plus avancés au monde et le fait d’avoir accès à cette installation nous a permis de voir la structure atomique 3D de la PETase dans des détails incroyables. Pouvoir voir le fonctionnement interne de ce catalyseur biologique nous a fourni les plans pour créer une enzyme plus rapide et plus efficace.
La clé de cette percée fut l’observation qu’à cette haute résolution, la PETase semble très similaire à l’enzyme cutinase, mais avec quelques différences notables. L’une d’entre elle était une zone active plus ouvert qui lui permettait d’accepter des polymères artificiels au lieu de variantes naturelles.
Cela suggère que la PETase a évolué dans un environnement où le PET est présent, de sorte que les chercheurs ont muté le site actif de la PETase pour se comporter davantage comme la cutinase, afin d’avoir davantage de preuves de cette théorie. En tentant de réduire son activité, ils l’ont en faite augmenté et au lieu que la PETase mutante s’avère inefficace à dégrader le PET, l’équipe a constaté le contraire, c’est-à-dire qu’elle a en fait obtenu de meilleurs résultats. Ainsi cette enzyme est devenue 20 % plus performante à transformer le plastique.
Selon M. McGeehan :
Le hasard joue souvent un rôle important dans la recherche scientifique fondamentale et notre découverte ici ne fait pas exception. Bien que l’amélioration soit modeste, cette découverte inattendue suggère qu’il y a de la place pour améliorer davantage ces enzymes, ce qui nous rapproche d’une solution de recyclage pour la montagne sans cesse croissante de plastiques mis au rebut.
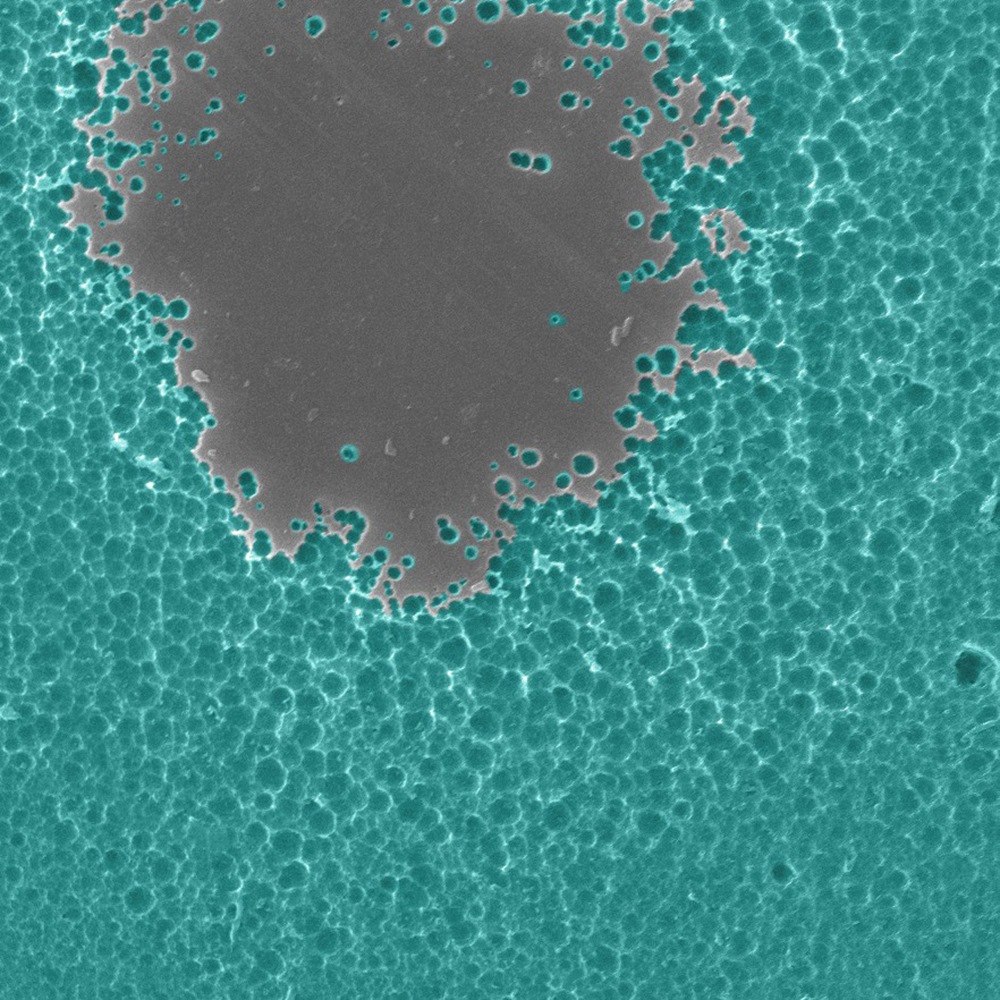
Une image au microscope électronique montrant l’interaction de l’enzyme (verte/ bleue) avec le plastique (gris). (H. P. Austin et col)
L’enzyme modifiée a l’avantage supplémentaire d’être capable de dégrader le polyéthylène furandicarboxylate (PEF), une alternative au PET qui a été lancée en remplacement des bouteilles de bière en verre. L’équipe travaille maintenant à optimiser l’enzyme modifiée pour la rendre encore plus efficace.
Selon M. McGeehan :
Le processus d’ingénierie est à peu près le même que pour les enzymes actuellement utilisées dans les détergents de lavage biologique et dans la fabrication de biocarburants, la technologie existe et il est tout à fait possible que dans les années à venir, nous voyons un processus industriellement viable pour transformer le PET et potentiellement d’autres substrats comme le PEF, Le PLA et le PBS retournent dans leurs blocs de construction d’origine afin qu’ils puissent être recyclés de façon durable.
L’étude publiée dans The Proceedings of the National Academy of Sciences : Characterization and engineering of a plastic-degrading aromatic polyesterase et présentée sur le site de l’université de Portsmouth : Engineering a plastic-eating enzyme.